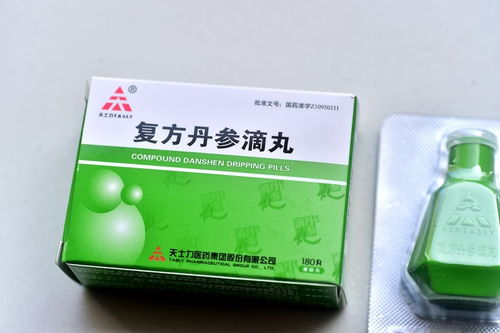
中医药国际化进程不断推进,中成药作为中医药的重要组成部分,其出海之路备受瞩目。其中,天津天士力制药集团的拳头产品——复方丹参滴丸的国际化征程,特别是其在美国食品药品监督管理局(FDA)的注册申请之路,一直被视为中成药走向国际高端市场的“风向标”。这条道路并非一帆风顺,近期其赴美进程再起波澜,折射出中成药出海所面临的普遍挑战与深层思考。
一、复方丹参滴丸的“美国梦”与漫漫征程
复方丹参滴丸源于中医经典方剂,主要用于冠心病、心绞痛等心血管疾病的治疗与预防。自上世纪90年代末,天士力便启动了该产品进军美国市场的计划,旨在通过FDA严格的临床试验和评审,获得在美国作为处方药上市的资格。这被业内视为一项开创性的尝试,因为若能成功,将意味着中成药首次以药品身份(而非膳食补充剂)进入全球最严苛的药品市场,其科学价值和临床疗效将得到国际主流医学体系的权威认可。
为此,天士力投入巨资,按照国际标准开展了多中心、随机、双盲、安慰剂对照的Ⅲ期临床试验。其评审过程漫长且曲折。虽然早期临床试验结果积极,但在关键的后续阶段,FDA对试验设计、终点指标、数据统计等方面提出了更高、更具体的要求,导致其补充试验和数据分析工作异常复杂。有关其临床试验数据需要进一步补充或澄清的消息传出,意味着最终的审批决定可能再次延迟,为该产品的“美国梦”蒙上了一层新的不确定性。
二、波澜再起的背后:中成药出海的共性难题
复方丹参滴丸的此番波澜,并非个案,而是中成药乃至整个中医药国际化进程中结构性难题的集中体现:
- 标准差异与“话语权”困境:中医药理论体系(如整体观、辨证论治)与现代西方医学的“病-药”对应、量化评价模式存在根本性差异。中成药多为复方,其“多成分、多靶点”的作用机制难以用单一的化学药评价标准完全解释和验证。如何设计出既符合国际科学规范,又能充分体现中医药特色的临床试验方案,是最大挑战。
- 质量控制与标准化难题:中药材的产地、种植、采收、炮制等环节的差异,直接影响最终成药的质量和成分稳定性。要达到FDA等机构对药品批次间高度一致性的严苛要求,需要从中药材源头到生产全链条建立可追溯、可量化的国际一流质量标准体系,这涉及庞大的产业链升级。
- 文化认知与市场接受度:即便通过了法规审批,如何让习惯了化学药的西方医生和患者理解并接受中成药的疗效逻辑和使用方法,是另一道市场门槛。这需要长期的学术推广、医生教育和文化沟通。
三、启示与未来路径
尽管前路崎岖,但复方丹参滴丸的探索具有不可磨灭的价值。它的每一步进展与挫折,都为后续者积累了宝贵的经验。其波澜也促使行业进行更深层的反思:
- 回归科学本质,创新研究范式:必须坚持以最严谨的现代科学研究方法,去阐释中成药的有效性和安全性。积极探索适合复方特点的“生物标志物”、“系统生物学”等新型评价模型,争取在国际规则框架下建立更合理的评价“话语权”。
- 夯实产业基础,实现全程可控:从种子种苗到患者手中,全面提升产业链的标准化、数字化、智能化水平,确保产品质量恒定、疗效可靠,这是国际化的根基。
- 多元化出海策略:在攻坚美国等高端处方药市场的可以并行推进以保健品、传统药物身份在东南亚、欧洲(根据传统草药产品指令)、非洲等已有认知基础的市场的注册,积累国际运营经验和品牌声誉。
- 加强国际合作与对话:积极与国际监管机构、科研院所、临床机构开展合作,增进相互理解,共同探索传统医学国际注册的可行路径和标准。
复方丹参滴丸赴美之路的波澜,是中成药国际化进程中的一个重要注脚。它既揭示了挑战的严峻性,也彰显了中国制药企业勇闯国际高端市场的决心。这条路注定需要耐心、智慧和持续的投入。它不仅仅是一个产品的上市问题,更是一场关于东西方医学对话、传统智慧与现代科技融合的深刻实践。无论最终结果如何,这一过程本身所推动的科研进步、质量提升和理念革新,都将为中国中医药产业的整体升级和国际化积累不可或缺的力量。中成药出海,道阻且长,行则将至。